رطوبت باقیمانده در هوای خشک، حتی در مقادیر ناچیز، میتواند کارایی تجهیزات و پایداری فرآیندهای حساس را بهطور محسوسی تحت تأثیر قرار دهد. 02146837072 - 09120253891
هوای خشک در بسیاری از صنایع بهعنوان یک محیط کنترلشده و پایدار شناخته میشود؛ محیطی که قرار است فاقد بخار آب بوده و شرایط یکنواختی برای فرآیندهای حساس فراهم کند. با این حال، در عمل همواره مقداری رطوبت باقیمانده در سیستم وجود دارد که میتواند عملکرد هوای خشک را تحت تأثیر قرار دهد. این رطوبت ممکن است ناشی از نشتیها، جذب سطحی در خطوط انتقال، عملکرد ناقص درایرها یا شرایط محیطی باشد. در این مقاله بهصورت تحلیلی به بررسی اثر رطوبت باقیمانده بر عملکرد هوای خشک در حوزههای مختلف صنعتی، آزمایشگاهی و تجهیزات دقیق پرداخته میشود.
ماهیت هوای خشک و مفهوم رطوبت باقیمانده
هوای خشک به هوایی گفته میشود که بخش عمده بخار آب آن حذف شده و نقطه شبنم آن بهطور محسوسی پایین آورده شده است. در سیستمهای صنعتی، نقطه شبنم معمولاً بهعنوان شاخص اصلی میزان رطوبت در نظر گرفته میشود. هرچه نقطه شبنم پایینتر باشد، میزان بخار آب موجود در هوا کمتر است.
رطوبت باقیمانده به آن میزان بخار آبی گفته میشود که پس از فرآیند خشکسازی همچنان در جریان هوا وجود دارد. این مقدار ممکن است در حد ppm یا حتی کمتر باشد، اما در کاربردهای حساس مانند ابزار دقیق، صنایع الکترونیک یا خطوط آنالیز گاز، همین مقدار اندک نیز میتواند پیامدهای قابلتوجهی ایجاد کند.
وجود رطوبت باقیمانده میتواند به دلایل مختلفی رخ دهد:
نخست، اشباع ناقص بسترهای جاذب در خشککنهای جذبی.
دوم، افت عملکرد درایرهای تبریدی در دماهای محیطی بالا.
سوم، میعان مجدد بخار آب در خطوط انتقال در اثر تغییرات دما و فشار.
در نتیجه، مفهوم «هوای خشک مطلق» در عمل کمتر تحقق مییابد و همواره باید میزان رطوبت باقیمانده بهدقت پایش شود.
تأثیر رطوبت باقیمانده بر فرآیندهای صنعتی
یکی از مهمترین حوزههایی که از رطوبت باقیمانده آسیب میبیند، فرآیندهای صنعتی حساس به خوردگی و واکنشهای شیمیایی ناخواسته است.
تشدید خوردگی در تجهیزات فلزی
حتی مقدار اندک رطوبت در هوای خشک میتواند زمینه تشکیل لایههای نازک آب روی سطوح فلزی را فراهم کند. این لایههای میکروسکوپی، بستر مناسبی برای واکنشهای الکتروشیمیایی ایجاد میکنند و در حضور اکسیژن، فرآیند اکسیداسیون فلزات سرعت میگیرد.
در خطوط ابزار دقیق، شیرآلات کنترلی و تجهیزات پنوماتیکی، این خوردگی تدریجی باعث کاهش عمر مفید تجهیزات و افزایش هزینههای نگهداری میشود.
اختلال در پوششدهی و رنگکاری
در صنایعی که از هوای خشک برای ایجاد محیط کنترلشده در رنگکاری یا پوششدهی استفاده میشود، وجود رطوبت باقیمانده میتواند موجب ایجاد حباب، پوستهشدن یا کاهش چسبندگی پوشش گردد. رطوبت در لایه زیرین میتواند هنگام خشکشدن نهایی تبخیر شده و ساختار سطحی را تخریب کند.
تأثیر بر فرآیندهای احتراقی
در برخی سیستمهای احتراقی دقیق، نسبت سوخت به هوا باید کاملاً کنترل شود. وجود بخار آب در هوای ورودی میتواند ظرفیت حرارتی مخلوط را تغییر داده و بر راندمان احتراق اثر بگذارد. در نتیجه ، بازده انرژی کاهش یافته و انتشار آلایندهها افزایش مییابد.
اثر رطوبت باقیمانده بر سیستمهای پنوماتیک و ابزار دقیق
سیستمهای پنوماتیکی به جریان هوای خشک و تمیز وابستهاند. رطوبت باقیمانده میتواند عملکرد این سیستمها را مختل کند.
کاهش کارایی عملگرهای پنوماتیکی
بخار آب موجود در هوا در فشارهای بالا متراکم شده و ممکن است در نقاط سردتر سیستم به مایع تبدیل شود. این میعان میتواند در سیلندرها و ولوها تجمع یافته و حرکت پیستونها را با مشکل مواجه کند. در دماهای پایین، حتی خطر یخزدگی نیز وجود دارد که عملکرد تجهیزات را متوقف میکند.
آسیب به سنسورها و تجهیزات اندازهگیری
در ابزارهای دقیق که برای اندازهگیری فشار، دبی یا ترکیب گاز طراحی شدهاند، رطوبت میتواند موجب خطای اندازهگیری شود. سنسورهای حساس به رطوبت ممکن است پاسخ نادرست ارائه دهند یا در طول زمان دچار انحراف شوند.
در صنایع دارویی و غذایی که دقت و تکرارپذیری اهمیت بالایی دارد، همین انحرافهای کوچک میتواند به عدم انطباق با استانداردهای کیفی منجر شود.
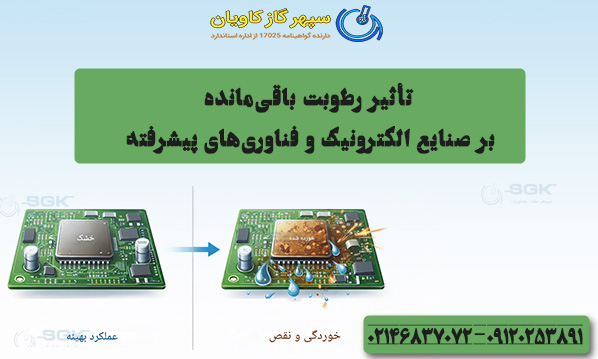
تأثیر رطوبت باقیمانده بر صنایع الکترونیک و فناوریهای پیشرفته
صنایع الکترونیک و نیمهرسانا از جمله حساسترین حوزهها نسبت به رطوبت هستند. حتی چند ppm بخار آب میتواند تأثیرات جدی ایجاد کند.
تخریب تدریجی قطعات الکترونیکی
رطوبت باقیمانده میتواند روی بردهای الکترونیکی میعان کند و باعث ایجاد مسیرهای رسانای ناخواسته شود. این موضوع احتمال اتصال کوتاه یا خوردگی مسیرهای مسی را افزایش میدهد.
در محیطهای تولید تراشههای نیمهرسانا، کنترل رطوبت در حد بسیار پایین انجام میشود؛ زیرا بخار آب میتواند در واکنشهای شیمیایی سطح ویفر سیلیکونی دخالت کرده و کیفیت لایهنشانی را تحت تأثیر قرار دهد.
کاهش پایداری در اتاقهای تمیز
در اتاقهای تمیز، هوای خشک برای کنترل ذرات و جلوگیری از واکنشهای ناخواسته استفاده میشود. وجود رطوبت باقیمانده میتواند موجب تجمع بار الکتریکی ساکن یا تغییر رفتار ذرات معلق شود. این امر بر دقت فرآیندهای میکروالکترونیک اثرگذار است.
چالشهای پایش و کنترل رطوبت باقیمانده
کنترل رطوبت باقیمانده تنها به نصب یک خشککن محدود نمیشود، بلکه نیازمند طراحی سیستماتیک و پایش مستمر است.
انتخاب فناوری مناسب خشکسازی
درایرهای تبریدی، جذبی و غشایی هرکدام مزایا و محدودیتهای خاص خود را دارند. برای کاربردهای عمومی، درایر تبریدی ممکن است کافی باشد، اما در کاربردهای بسیار حساس، استفاده از خشککنهای جذبی با نقطه شبنم بسیار پایین ضروری است.
اهمیت پایش نقطه شبنم
نصب سنسورهای دقیق نقطه شبنم در نقاط کلیدی سیستم به شناسایی افزایش ناگهانی رطوبت کمک میکند. پایش پیوسته امکان واکنش سریع در صورت افت عملکرد سیستم خشکسازی را فراهم میسازد.
طراحی مناسب خطوط انتقال
عایقکاری خطوط، جلوگیری از نقاط سرد، شیببندی مناسب برای تخلیه میعانات و استفاده از متریال مقاوم به خوردگی از جمله اقداماتی است که میتواند اثرات رطوبت باقیمانده را کاهش دهد.
پیامدهای اقتصادی رطوبت باقیمانده
وجود رطوبت در هوای خشک تنها یک مسئله فنی نیست، بلکه پیامدهای اقتصادی قابلتوجهی نیز دارد.
افزایش هزینههای تعمیر و نگهداری، کاهش عمر تجهیزات، توقفهای ناخواسته تولید و افت کیفیت محصول از جمله هزینههای مستقیم و غیرمستقیم ناشی از کنترل نامناسب رطوبت هستند.
در بسیاری از موارد، سرمایهگذاری در یک سیستم خشکسازی پیشرفته و پایش دقیق، در بلندمدت بسیار مقرونبهصرفهتر از جبران خسارات ناشی از رطوبت خواهد بود.
رطوبت باقیمانده در هوای خشک، هرچند در نگاه اول ناچیز به نظر میرسد، میتواند اثرات گستردهای بر عملکرد تجهیزات، کیفیت فرآیندها و پایداری سیستمهای صنعتی داشته باشد. این رطوبت قادر است خوردگی را تسریع کند، دقت ابزارهای اندازهگیری را کاهش دهد، فرآیندهای حساس الکترونیکی را مختل سازد و هزینههای نگهداری را افزایش دهد.
بنابراین، مدیریت رطوبت باقیمانده باید بهعنوان بخشی جداییناپذیر از طراحی و بهرهبرداری سیستمهای هوای خشک در نظر گرفته شود. استفاده از فناوری مناسب خشکسازی، پایش مداوم نقطه شبنم و طراحی صحیح خطوط انتقال، سه رکن اساسی در کنترل این چالش به شمار میآیند.